
Guia de Estudos
Que bom ter você por aqui no Hypnare! Sabemos que a sua jornada para se tornar um anestesiologista de excelência é intensa e cada detalhe na prática clínica faz a diferença.
Nesse caminho, os anestésicos locais são muito mais que um fármaco: são a sua principal ferramenta para garantir a segurança e o conforto do paciente. Dominar seu uso é o que constrói a verdadeira confiança.
Espero que o conteúdo do site esteja agregando valor à sua formação e que você compartilhe essas dicas com seus colegas residentes. Agora, vamos continuar firmes e aprender de vez tudo sobre anestésicos locais. Combinado?
A Estrutura por Trás da Ação: Química, pKa e pH
Todos os anestésicos locais (AL) partilham uma estrutura química fundamental de três partes: um grupo lipofílico (anel de benzeno), uma cadeia intermediária (do tipo éster ou amida) e um grupo hidrofílico (amina). Para não se confundir, lembre-se: anestésicos do tipo éster têm um “i” no nome (procaína), enquanto os do tipo amida têm dois “i’s” (lidocaína).
Esses medicamentos agem bloqueando os canais de sódio na membrana dos neurônios. Para isso, a molécula precisa estar em sua forma não ionizada (lipossolúvel) para atravessar a membrana. Dentro da célula, ela se reioniza e, em sua forma ionizada, bloqueia o canal por dentro, impedindo a transmissão do impulso nervoso.
O pKa de um AL é o pH no qual 50% do fármaco está na forma ionizada e 50% na não ionizada. A relação entre pKa e pH define a clínica:
- Início de Ação: Quanto mais próximo o pKa do pH fisiológico (7,4), mais rápida a ação.
- Acidose Tecidual: Em tecidos infectados (pH baixo), o AL fica predominantemente ionizado, não atravessa a membrana e a anestesia falha.
- Aprisionamento Iônico (Ion Trapping): Fenômeno crucial em obstetrícia. O AL atravessa a placenta na forma não ionizada. Se o feto estiver em acidose, o fármaco se ioniza e, por não conseguir retornar pela barreira lipídica da placenta, acumula-se, aumentando o risco de toxicidade fetal.
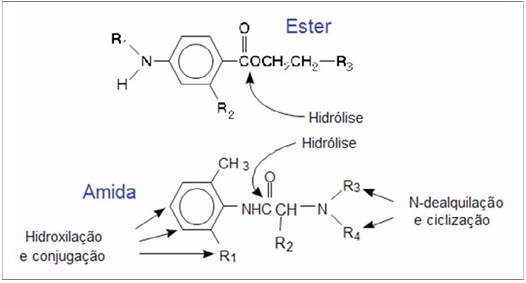
Figura 1. Metabolismo dos anestésicos locais. As amidas sofrem metabolismo hepático de fase I (inclui hidroxilação, N-dealquilação e metilação) e de fase II (compreende a conjugação com aminoácidos como a glicina). Ésteres são rapidamente hidrolisados no plasma.
É importante ressaltar que os ALs exibem um bloqueio uso-dependente, o que significa que sua afinidade pelos canais de sódio varia conforme o estado do canal. Eles têm maior afinidade por canais no estado aberto, seguida pelo estado inativado e, por último, pelo estado de repouso. Essa preferência explica por que nervos que disparam com mais frequência (como as fibras da dor tipo A-delta e C) são mais suscetíveis à ação do anestésico.
A química por trás dessas moléculas é um fator crucial em sua toxicidade. A bupivacaína, por exemplo, é uma mistura racêmica, contendo dois isômeros (quiralidade): o levógiro S(-) e o dextrógiro R(+). O isômero R(+) é o principal responsável pela cardiotoxicidade e neurotoxicidade. Por isso, a levobupivacaína foi desenvolvida, consistindo apenas no isômero S(-), o que a torna uma opção mais segura.
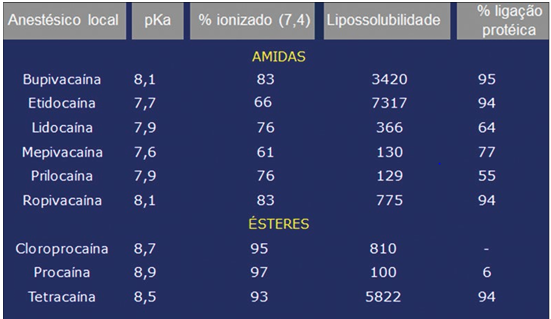
Figura 2. pKa (pH em que 50% da solução está na forma de base livre e 50% na forma ionizada); porcentagem na forma ionizada no pH fisiológico; lipossolubilidade e porcentagem de ligação proteica dos principais anestésicos locais.
Metabolismo e Biotransformação
A forma como um anestésico local é metabolizado é fundamental para sua duração e toxicidade.
- Anestésicos do tipo Éster: São metabolizados rapidamente no plasma por uma enzima chamada pseudocolinesterase plasmática. O produto final é o ácido para-aminobenzóico (PABA), um metabólito que é a principal causa das reações alérgicas. A cloroprocaína é considerada o anestésico local menos tóxico devido à sua rápida hidrólise.
- Anestésicos do tipo Amida: A biotransformação ocorre no fígado, por meio do sistema enzimático do citocromo P450. A metabolização é mais lenta, o que contribui para sua maior duração de ação e aumenta o risco de toxicidade em neonatos e pacientes com insuficiência hepática, nos quais a degradação é ainda mais lenta.
Potência, Duração e Absorção Sistêmica
A potência de um AL está diretamente relacionada à sua lipossolubilidade. Quanto mais lipossolúvel, maior a capacidade de penetração na membrana nervosa e, consequentemente, maior a potência.
- Ordem de Potência (maior para a menor):
- Bupivacaína / Levobupivacaína / Ropivacaína: Mais potentes.
- Lidocaína / Mepivacaína: Potência intermediária.
- Procaína: Menor potência.
A absorção sistêmica e, consequentemente, a chance de toxicidade, varia de acordo com o local de aplicação. Quanto mais vascularizada a região, mais rápida e maior será a absorção.
- Ordem de Absorção Sistêmica e Risco de Toxicidade (da maior para a menor):
- Bloqueio Intercostal: É o local de maior absorção sistêmica.
- Bloqueio Caudal
- Bloqueio Peridural Lombar
- Bloqueio do Plexo Braquial
- Bloqueio Ciático-Femoral
Detalhes sobre os Anestésicos Locais Comuns:
- Lidocaína: É o padrão-ouro de potência intermediária e duração média, sendo o AL mais utilizado. Sua duração de ação é de aproximadamente 45 a 90 minutos.
- Bupivacaína: Conhecida por sua alta potência e longa duração (4 a 8 horas), é ideal para procedimentos longos e controle da dor pós-operatória. No entanto, é a mais cardiotóxica.
- Levobupivacaína e Ropivacaína: São isômeros da bupivacaína, desenvolvidos para serem menos cardiotóxicos. A Ropivacaína, em particular, se destaca por duas características importantes: o bloqueio diferencial, agindo mais nas fibras sensitivas do que nas motoras, tornando-a excelente para analgesia de parto sem comprometer a capacidade de movimento; e um efeito vasoconstritor intrínseco em doses clinicamente relevantes, o que pode reduzir a absorção sistêmica e prolongar discretamente sua ação, diferentemente da bupivacaína. A duração de ação de ambos é de aproximadamente 4 a 8 horas.
- Procaína: Um anestésico do tipo éster, de curta duração (30 a 60 minutos) e menos potente. É menos comum devido ao risco de reações alérgicas.
Sintomas Neurológicos Transitórios (SNT) com Lidocaína
É de suma importância que o residente conheça os Sintomas Neurológicos Transitórios (SNT), uma complicação associada principalmente ao uso de lidocaína em raquianestesia.
O SNT é caracterizado por dor nas pernas ou nádegas que se manifesta entre 6 a 24 horas após a recuperação do bloqueio neuroaxial. Os sintomas são temporários e, geralmente, desaparecem em 1 a 7 dias. Acredita-se que a lidocaína possa causar uma irritação direta das raízes nervosas.
Sensibilidade das Fibras, Bloqueio Diferencial e Níveis de Bloqueio
A magia dos bloqueios reside em entender que nem todas as fibras nervosas são iguais. A sensibilidade ao anestésico depende do diâmetro e da mielinização da fibra.
- Ordem de Bloqueio (da mais sensível para a menos):
- Fibras B (Autonômicas): Finas e pouco mielinizadas. Responsáveis pelo tônus simpático (vasodilatação). São as primeiras a serem bloqueadas.
- Fibras C e A-delta (Dor e Temperatura): Finas e amielínicas ou pouco mielinizadas.
- Fibras A-beta (Tato e Pressão).
- Fibras A-alfa (Motoras): Grossas e muito mielinizadas. São as últimas e mais resistentes ao bloqueio.
Essa sequência explica a progressão clínica de um bloqueio neuroaxial: o paciente sente calor (bloqueio simpático), depois perde a sensibilidade à dor e, por fim, a função motora.
- Níveis de Bloqueio: O bloqueio simpático geralmente se estende de 2 a 6 dermátomos acima do bloqueio sensitivo, que, por sua vez, fica 2 dermátomos acima do bloqueio motor.
- Bloqueio Diferencial: É a capacidade de bloquear seletivamente as fibras de dor (sensitivas) com mínimo impacto nas fibras motoras. A ropivacaína e a bupivacaína, em baixas concentrações, são mestres nisso, sendo ideais para analgesia de parto.
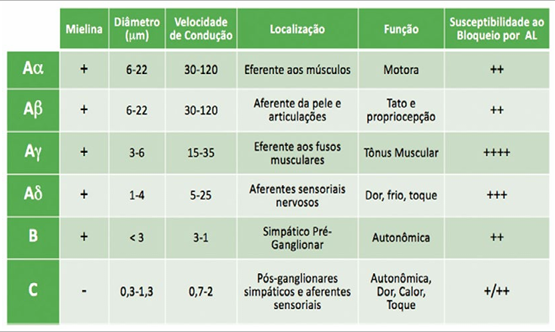
Figura 3. Classificação das fibras nervosas.
Efeitos Colaterais e Tratamento da Toxicidade Sistêmica (LAST)
A toxicidade sistêmica por anestésicos locais (LAST, do inglês Local Anesthetic Systemic Toxicity) ocorre quando o medicamento atinge a corrente sanguínea em concentrações elevadas, afetando principalmente os sistemas nervoso central (SNC) e cardiovascular (SCV).
- Sinais e Sintomas: É vital lembrar que a toxicidade do SNC geralmente se manifesta antes da cardiotoxicidade. Sinais neurológicos incluem gosto metálico, zumbido, agitação e convulsões. Se esses sinais aparecerem, é provável que a toxicidade cardiovascular (bradicardia, arritmias, hipotensão e, em casos graves, parada cardíaca) seja iminente.
Tratamento da LAST: Um Guia Passo a Passo
- Ações Imediatas:
- Pare a injeção e chame ajuda!
- Manejo da Via Aérea: Ventile com O₂ a 100%. A hiperventilação controlada ajuda, mas evite a acidose, que potencializa a toxicidade.
- Inicie a RCP se houver PCR. Acione a equipe de ECMO precocemente em casos refratários.
- Tratamento das Convulsões:
- Benzodiazepínicos são a primeira linha. Evite propofol se houver instabilidade hemodinâmica.
- Terapia com Emulsão Lipídica (Intralipid 20%): O Antídoto
Esta é a terapia essencial para o colapso cardiovascular. Seu mecanismo é multifatorial, baseado em duas teorias principais que provavelmente atuam em conjunto:
- “Pia Lipídica” (Lipid Sink): A teoria mais clássica. A emulsão infundida cria um compartimento lipídico intravascular expandido que “sequestra” as moléculas lipossolúveis do anestésico local, retirando-as de seus sítios de ligação no coração e no cérebro e acelerando sua redistribuição para órgãos inativos.
- Efeito Metabólico e Inotrópico Direto: Diretrizes mais recentes enfatizam que os lipídios também fornecem um substrato energético vital (ácidos graxos) para o miocárdio, que está sofrendo de inibição do seu metabolismo energético causado pelo AL. Isso ajuda a restaurar a função mitocondrial e a produção de ATP, melhorando diretamente a contratilidade cardíaca.
- Protocolo:
- Bolus: Se > 70 kg, 100 ml; se < 70 kg, 1,5 ml/kg (em 2-3 min).
- Infusão: Iniciar com 0,25 ml/kg/minuto.
- Repetir Bolus: Pode ser repetido até 2 vezes.
- Dose Máxima: Não exceder 12 ml/kg.
- Manejo das Arritmias e Suporte Hemodinâmico:
- Adrenalina: Use doses reduzidas (< 1 mcg/kg).
- Antiarrítmico de escolha: Amiodarona.
- Medicamentos a serem EVITADOS e o porquê:
- Vasopressina: Pode piorar a função pulmonar e o fluxo coronariano.
- Bloqueadores de Canais de Cálcio e Betabloqueadores: Agravam a depressão miocárdica e a bradicardia já induzidas pelo AL.
- Lidocaína (ou outro AL): Adiciona mais toxicidade ao cenário.
Conclusão: O Próximo Passo na Sua Jornada
Dominar os anestésicos locais é um dos superpoderes do anestesiologista. O que você leu aqui é a base para transformar a teoria em segurança e confiança no centro cirúrgico, mas a jornada rumo à excelência continua.
Não deixe este conhecimento guardado. Coloque-o em movimento!
- Teste seu Raciocínio Clínico: Use nosso banco de questões sobre o tema. A melhor maneira de aprender não é apenas ler, é resolver problemas.
- Memorize o que Salva Vidas: Use a técnica de flashcards para fixar o protocolo de LAST. Em uma crise, você não terá tempo para consultar, terá que agir.
- Continue sua Exploração: O Hypnare é seu parceiro de estudos. Aproveite que está aqui e mergulhe em outros temas que desafiem você.
Sua dedicação hoje é a tranquilidade do seu paciente amanhã. Continue estudando, questionando e crescendo. Nos vemos no próximo artigo!
Leitura Complementar:
Barash Anestesia
Miller Anestesia
SAESP Anestesia
Bases do Ensino da Anestesiologia
